在医药中间体领域,一个分析方法的可靠性,直接决定产品的放行与否.而GMP对方法验证(Validation)与方法转移(Transfer)的要求近乎苛刻:方案必须覆盖ICH Q2(R1)所有参数,数据必须完整、可追溯,任何偏差都需闭环处理,最终报告需经严格审批.手工或半手工模式下,这几乎是一项“不可能完成的任务”.
如何破局?答案是:用LIMS构建一套GMP原生的方法全生命周期管理体系.
传统模式存在三大致命缺陷:
📄 方案与执行脱节:Word方案与Excel数据分离,无法证明每一步都按方案执行;
🔍 数据追溯困难:原始图谱、计算过程散落在不同电脑,审计时“找不到、对不上”;
✍️ 签名与审批滞后:纸质签名易遗漏,电子审批无法律效力,不符合21 CFR Part 11.
任何一个环节出错,都可能导致整个验证/转移活动被判无效.
1. 结构化方案模板,确保无一遗漏
LIMS内置符合ICH Q2(R1)的验证方案模板,强制要求填写专属性、线性、范围、准确度、精密度、检测限/定量限、耐用性等所有参数.用户无法跳过任一必填项,从源头保证方案完整性.
2. 全生命周期数据绑定,构建完整证据链
从方案创建、样品制备、仪器运行到结果计算,所有操作和产出(包括HPLC图谱、称量记录、计算表格)自动关联至同一验证/转移任务,形成一个不可分割的数字档案.审计员可一键调阅全部证据.
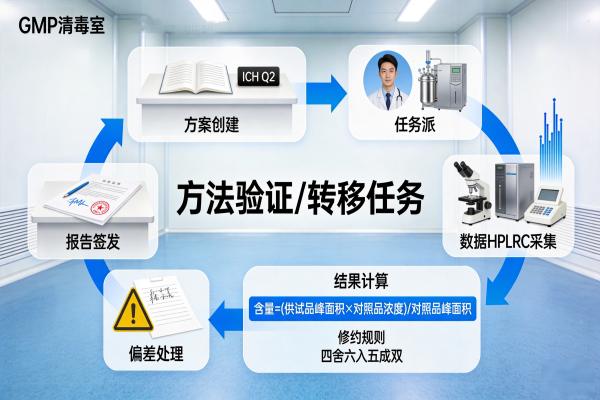
3. 电子签名与审计追踪,满足法规硬性要求
关键节点(如方案批准、报告审核、最终签发)均需相关责任人使用合规的电子签名确认.系统同步记录完整的审计追踪(Audit Trail),包含谁、何时、做了什么、修改了什么,完全满足GMP及21 CFR Part 11对数据完整性的要求.
某华东知名CDMO企业(专注高活性医药中间体)上线LIMS方法管理模块后,实现质的飞跃:
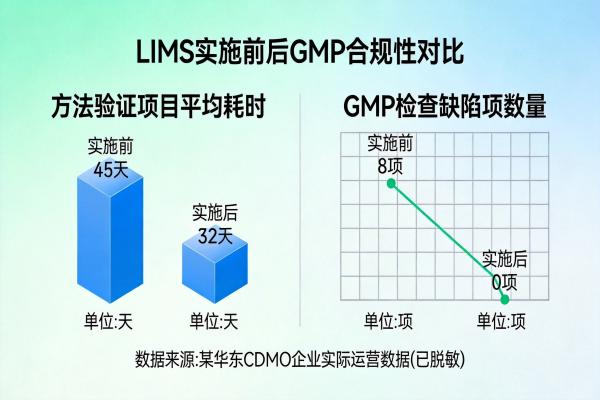
🛡️ NMPA GMP检查“零缺陷”:在最近一次符合性检查中,方法验证与转移部分获检查员高度认可;
⏱️ 项目周期缩短30%:因无需返工整理资料,方法转移效率大幅提升;
🔒 数据完整性100%达标:所有历史项目均可秒级追溯,彻底告别“补记录”时代.
其QA总监坦言:“现在我们不是‘准备’检查,而是随时‘欢迎’检查.”
Excel或共享文件夹看似灵活,实则隐患重重:
⚠️ 文件可随意复制、修改,无法保证唯一性和真实性;
⚠️ 无权限控制,实习生也能修改关键方案;
⚠️ 无审计追踪,无法证明数据未被篡改.
GMP要求的是一个受控的、封闭的、可验证的数字化环境,而这正是专业LIMS的核心价值所在——它不是一个工具,而是一个合规的“操作系统”.
在生命科学领域,合规不是成本,而是信任的基石.LIMS,正是为这块基石提供数字化支撑的不二之选.
正在了解 LIMS实验室信息管理系统 相关解决方案?
支持低代码定制开发、可源码交付与私有化部署,欢迎咨询!
咨询电话:15978966810
30天倒计时!用LIMS快速完成人员授权、设备状态、数据完整性三大核心项自查,附真实过审案例,助您顺利通过CNAS/CMA复评审。
展示针对特定法规和检测流程的深度定制开发过程与成果。通过动态配置检测项、智能判定结果、自动生成合规报告,轻松满足RoHS/REACH等严苛要求。附真实系统功能截图。
详解LIMS如何通过能力矩阵、仪器状态联动、动态负载均衡,在确保CNAS/CMA合规的前提下,将仪器利用率提升至82%,任务完成时间缩短40%。
分享针对科研人员特点的沟通、培训和激励策略,解决“人”的问题。通过尊重科研文化、简化操作流程、建立正向反馈,成功实现LIMS系统全员支持与高效使用。
详解LIMS如何与钉钉、企业微信集成,实现样品收样、检测、出报告等关键节点自动推送,减少70%客户咨询电话,提升服务体验。