收样管理是LIMS实验室信息管理系统落实CNAS对“样品处置受控”要求的第一道防线,也是客服与检测流程衔接的关键节点。重庆壹博LIMS基于CNAS-CL01:2018 第7.4条(样品处置)及第4.1条(公正性)要求,构建覆盖“人、机、料、法、环、审”全要素的数字化收样平台,实现样品“接得准、登得清、存得稳、转得明、毁得可溯”,彻底杜绝丢失、混淆、错漏等风险。
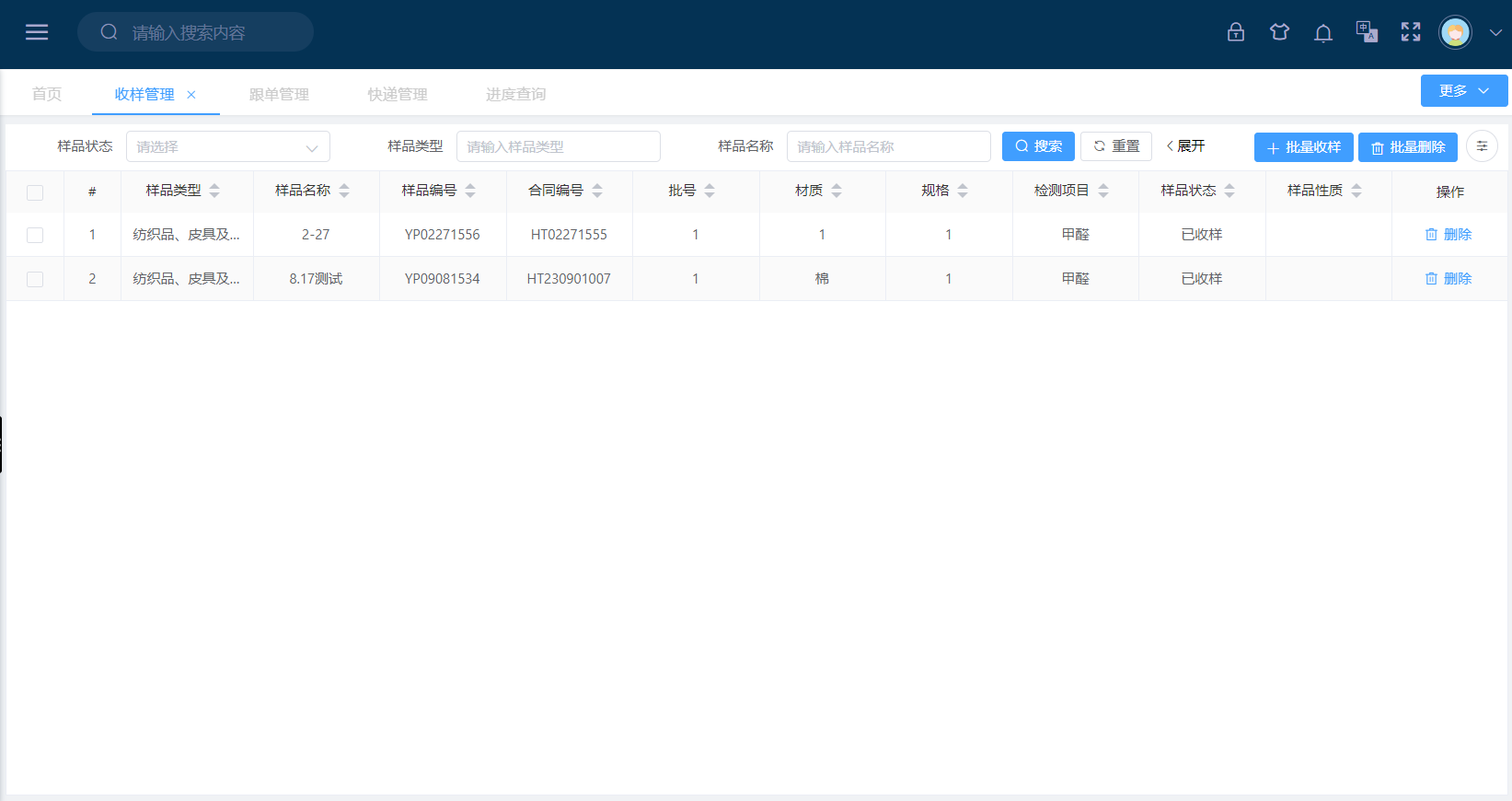
客服人员通过LIMS统一入口完成样品接收,系统自动执行:
• 唯一编号生成:按规则自动生成样品ID(如 SY-2025-00123),全局唯一不可重复;
• 客户信息关联:自动带出委托方、合同、测试申请表,避免手工录入错误;
• 属性结构化录入:名称、数量、形态(固/液/气)、颜色、气味、危险性标识等字段标准化;
• 异常情况记录:如包装破损、标签脱落、温度超标等,强制填写备注并拍照留证;
• 二维码标签打印:一键打印含样品ID的二维码标签,粘贴后扫码即可追溯全流程。
样品一旦登记,即进入受控生命周期:
• 暂存管理:指定保存位置(冰箱/常温柜/危化品柜)、温湿度要求,系统监控环境合规性;
• 流转交接:从客服移交至制样/检测人员时,需双方扫码确认,记录交接人与时间;
• 状态可视化:实时显示“已接收→待制样→检测中→报告完成→已归还/已销毁”;
• 超期预警:临近保存期限或客户要求交付日,自动提醒处理,防止过期失效。
任何环节均可通过样品ID反向追溯操作记录,满足审计要求。
不同实验室收样场景差异显著,LIMS提供灵活配置:
• 快递收样:登记快递单号,自动对接物流信息,异常包裹标红预警;
• 现场收样:移动端APP支持外勤人员现场拍照、定位、录入,数据实时同步;
• 批量收样:支持Excel模板导入或扫描枪批量扫码登记,提升效率;
• 盲样管理:自动隐藏客户信息,生成双编码(真实码+盲样码),保障检测公正性。
所有场景均在同一平台管理,数据统一、流程一致。
CNAS-CL01:2018 第7.4.1–7.4.5 条明确规定样品应“标识清晰、防止混淆、条件受控、处置可溯”。LIMS收样管理内嵌合规控制点:
• 自动校验样品标识唯一性
• 强制记录保存条件与环境参数
• 销毁操作需双人审批并留痕
• 所有操作日志不可篡改,保留至少6年
评审专家可一键导出某样品的完整履历,作为体系有效运行的直接证据。
无论是食品、环境、医药还是材料实验室,收样字段与流程各不相同。LIMS提供可视化配置平台,无需代码即可:
• 自定义样品属性字段(如批次号、生产日期、采样点位)
• 设置不同样品类型的保存规则与预警阈值
• 配置收样审批流(如危化品需安全员确认)
• 设计专属收样报表(日收样量、异常率、客户分布)
支持私有化部署与完整源码交付,保障长期自主可控。
正在了解 LIMS实验室信息管理系统 相关解决方案?
支持低代码定制开发、可源码交付与私有化部署,欢迎咨询!
咨询电话:15978966810
深度解析LIMS与RPA机器人流程自动化结合方案,如何消除实验室重复性手工操作,实现数据录入、报告生成等环节自动化,助力检测机构降本增效,提升运营效率。
实验室OOS调查动辄耗时数周?本文详解壹博LIMS如何通过标准化流程、自动化任务分派与电子记录,将OOS调查周期缩短50%以上,加速产品放行,满足GMP合规要求。
详解LIMS与ERP系统集成实战方法,实现采购、库存与检测数据无缝流转,提升实验室运营效率。含真实案例与技术要点。
从申购、入库、领用到报废,LIMS系统实现耗材全生命周期闭环管理,有效降低试剂成本20%,杜绝过期浪费。
低代码定制开发支持直接对接色谱仪、光谱仪等精密设备,通过IoT模块自动抓取原始数据,杜绝人工录入错误与人为篡改,确保数据完整性符合ALCOA+原则。