制样管理是LIMS实验室信息管理系统确保检测结果代表性与准确性的关键环节。重庆壹博LIMS严格遵循CNAS-CL01:2018 第7.7条(确保结果有效性)要求,基于“人、机、料、法、环、审”六要素构建数字化制样平台,对样品的切割、研磨、稀释、均质、封装等预处理过程进行标准化、可追溯、受控化管理,杜绝因制样不规范导致的数据偏差或无效检测。
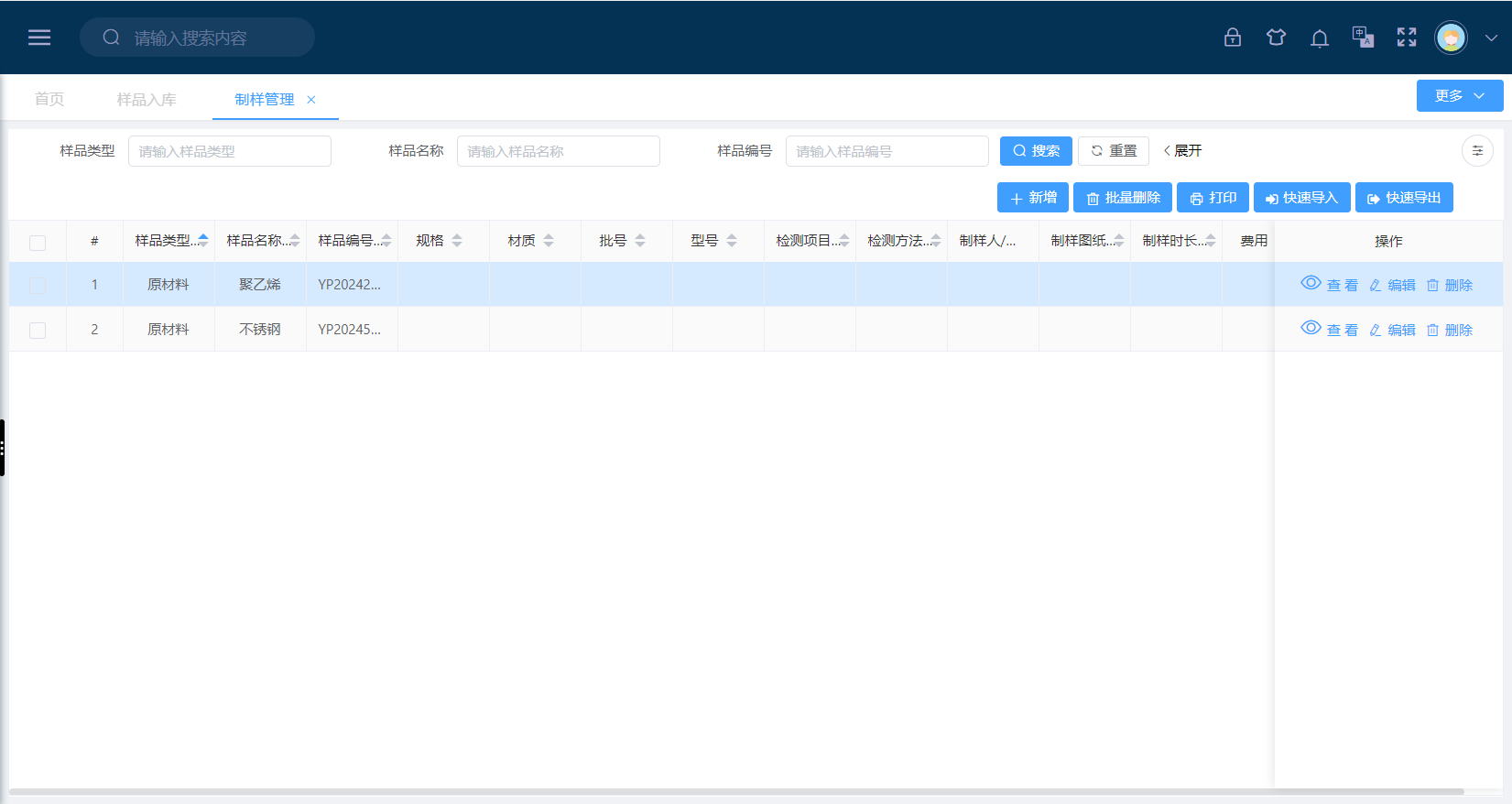
LIMS制样管理模块将传统依赖经验的操作转化为标准化流程:
• 母样自动关联:从已入库样品中选择待制样对象,系统带出原始信息;
• 制样方法绑定:根据检测项目自动匹配SOP(如GB/T 5009.3-2016 固体样品粉碎);
• 参数结构化录入:记录粒径、重量、体积、稀释倍数、均质时间等关键参数;
• 设备与耗材登记:关联使用的粉碎机、天平、移液器及批次号,实现设备溯源;
• 环境条件记录:自动采集或手动录入温湿度,确保制样环境合规。
所有操作强制按规程执行,减少人为随意性。
一次制样常产生多个子样用于不同检测项目。LIMS自动建立清晰的谱系关系:
• 唯一子样ID生成:如 ZY-2025-00123-A、ZY-2025-00123-B;
• 母子样关联图谱:点击任一子样,可反向追溯至原始母样及制样记录;
• 用途明确标注:每个子样绑定具体检测项目(如“A样→重金属,B样→农残”);
• 重量平衡校验:系统自动计算母样总重与各子样之和是否匹配,偏差超限预警。
评审专家可一键还原整个制样过程,验证数据逻辑一致性。
制样是误差高发环节,LIMS内嵌多重质控机制:
• SOP强制执行:未按标准方法操作,系统禁止提交;
• 人员资质校验:仅授权人员可执行特定制样任务(如危化品处理);
• 交叉污染防控:记录设备清洗状态,高风险样品需使用专用器具;
• 异常留痕:如样品洒落、称量超差,需填写原因并拍照,触发复样流程。
所有质控动作自动纳入质量体系运行证据链。
制样完成即自动触发后续流程:
• 子样状态更新为“待检测”,任务推送至对应检测员;
• 制样参数(如稀释倍数)自动带入检测原始记录模板;
• 报告编制时可直接引用制样方法与条件,避免重复录入;
• 若检测结果异常,可快速回溯制样环节排查原因。
打通“制样→检测→报告”数据链,保障结果完整性。
不同行业制样差异显著:
• 食品需均质化处理,环境样品需过滤浓缩,金属材料需线切割……
LIMS提供可视化配置平台,无需代码即可:
• 自定义制样方法库与SOP模板
• 设置不同样品类型的默认参数与必填项
• 配置母子样生成规则(1母→N子)
• 设计制样绩效报表(人均日处理量、异常率、设备利用率)
支持私有化部署与完整源码交付,满足信创与长期运维需求。
正在了解 LIMS实验室信息管理系统 相关解决方案?
支持低代码定制开发、可源码交付与私有化部署,欢迎咨询!
咨询电话:15978966810
深入解析LIMS权限体系的三层架构(功能、数据、操作),打破“一刀切”授权困局,实现“最小权限”原则下的灵活授权。
清晰界定LIMS与ELN的核心定位与功能边界,指导科研实验室和研发机构根据业务性质(检测vs研发)科学选型,避免重复建设与投资浪费。
深度解析LIMS与RPA机器人流程自动化结合方案,如何消除实验室重复性手工操作,实现数据录入、报告生成等环节自动化,助力检测机构降本增效,提升运营效率。
实验室OOS调查动辄耗时数周?本文详解壹博LIMS如何通过标准化流程、自动化任务分派与电子记录,将OOS调查周期缩短50%以上,加速产品放行,满足GMP合规要求。
详解LIMS与ERP系统集成实战方法,实现采购、库存与检测数据无缝流转,提升实验室运营效率。含真实案例与技术要点。